|
2. მოლეკულების მასა. ავოგადროს რიცხვი
წყლის მოლეკულის მასა. ცალკეული მოლეკულებისა და ატომების მასები ძალიან მცირეა. მაგალითად 1გ წყალი შეიცავს 3.7 · 10 22 მოლეკულას. მაშასადამე ერთი მოლეკულის მასა

ასეთივე რიგისაა სხვა ნივთიერებათა მოლეკულების მასაც, გარდა ორგანულ ნივთიერებათა იმ უზარმაზარი მოლეკულებისა, რომლებიც ათასობით ატომს შეიცავს.
ფარდობითი მოლეკულური მასა. რადგან მოლეკულების მასა ძალიან მცირეა, ამიტომ უმჯობესია გამოთვლისას ვისარგებლოთ მასის არა აბსოლუტური, არამედ ფარდობითი მნიშვნელობით. საერთაშორისო შეთანხმების მიხედვით (როგორც ეს ქიმიის კურსიდან ვიცით) ყველა მოლეკულისა და ატომის მასას ადარებენ ნახშირბადის ატომის მასის 1/12-ს (ატომური მასების ე.წ. ნახშირბადური სკალა). ნივთიერების ფარდობითი მოლეკულური (ან ატომური) მასა (Mფ) ეწოდება მოცემული ნივთიერების მოლეკულის (ან ატომის) მასის (m0) ფარდობას ნახშირბადისატომის მასის (m0C) 1/12-თან:
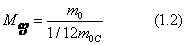
Mფ სიდიდეს დასახელება არ აქვს.
ამჟამად ყველა ქიმიური ელემენტის ფარდობითი ატომური მასა დიდი სიზუსტითაა გაზომილი. თუ შევკრებთ მოლეკულის შედგენილობაში შემავალ ატომთა ფარდობით მასებს, მივიღებთ ფარდობით მოლეკულურ მასას.
ნივთიერების რაოდენობა. რაც მეტია ატომების ან მოლეკულების რიცხვი მაკროსკოპულ სხეულში, ცხადია, მით მეტ ნივთიერებას შეიცავს მოცემული სხეული. მაკროსკოპულ სხეულში უამრავი მოლეკულაა. ამიტომ ვლაპარაკობთ ატომების ან მოლეკულების არა აბსოლუტურ, არამედ ფარდობით რიცხვზე.
მიღებულია, მოცემული სხეულის მოლეკულების ან ატომების რიცხვი შევადაროთ 0,012კგ ნახშირბადის ატომების რიცხვს. სხეულში ატომების ან მოლეკულების ფარდობითი რიცხვი ხასიათდება განსაკუთრებული სიდიდით რომელსაც ნ ი ვ თ ი ე რ ე ბ ი ს რ ა ო დ ე ნ ო ბ ა ეწოდება. ნივთიერების რაოდენობა ν (ბერძნული ასო, იკითხება „ნიუ") ეწოდება მოცემული სხეულის მოლეკულათა რიცხვი(N) ფარდობას 0,012კგ ნახშირბადის ატომების რიცხვთან (NA).

თუ ვიცით ν ნივთიერების რაოდენობა და NA რიცხვი, გავიგებთ მოლეკულის N რიცხვს ნივთიერებაში. ნივთიერების რაოდენობას გამოსახავენ მოლებით. მოლი ნივთიერების რაოდენობაა, რომელიც შეიცავს იმდენივე მოლეკულას, რამდენი ატომიცაა 0,012 კგ. ნახშირბადში. თუ ნივთიერების რაოდენობაა 2,5 მოლი, ეს ნიშნავს, რომ მოლეკულების რიცხვი სხეულში 2,5-ჯერ მეტია, ვიდრე ატომების რიცხვი 0,012კგ ნახშირბადში. ნივთიერების რაოდენობის საზომ ერთეულად კილომოლიც იხმარება.
1კ მოლი=103 მოლი.
ავოგადროს რიცხვი. მოლეკულების ან ატომების რიცხვს ერთ მოლ ნივთიერებაში(NA) ავოგადროს რიცხვი ეწოდება. (XIXსაუკუნის იტალიელი მეცნიერის პატივსაცემად). მოლის განსაზღვრის თანახმად ავოგადროს რიცხვი ერთი და იგივეა ყველა ნივთიერებისათვის და, კერძოდ, ტოლია ატომთა რიცხვისა, რომელსაც ნახშირბადის მოლი, ე.ი 0,012კგ ნახშირბადი შეიცავს. ავოგადროს რიცხვის განსაზღვრისათვის საჭიროა ვიპოვოთ ნახშირბადის ერთი ატომის(ან სხვა რომელიმე ატომის) მასა. მისი რამდენამდე მიახლოებითი შეფასება შეიძლება ისევე, როგორც შევაფასეთ წყლის მოლეკულის მასა(უფრო ზუსტი მეთოდი დამყარებულია ელქტრომაგნიტურ ველში იონთა კონების გადახრაზე). გაზომვებით ვღებულობთ, რომ ნახშირბადის ატომის მასა  მაშინ ავოგადროს რიცხვი მაშინ ავოგადროს რიცხვი

დასახელება მოლი-1 მიუთითებს, რომ NA ატომების რიცხვია ნებისმიერი ნივთიერების ერთ მოლში. თუ ნივთიერების რაოდენობა ν=2,5 მოლს მაშინ მოლეკულების რიცხვი სხეულში  ატომების რიცხვი კილომოლში ტოლია ატომების რიცხვი კილომოლში ტოლია  -ისა არსებობს ავოგადროს რიცხვის განსაზღვრის ბევრი ისეთი მეთოდი რომლებიც არ საჭიროებს ატომის მასის პოვნას. ყველა ეს მეთოდი ერთსა და იმავე შედეგს გვაძლევს. ავოგადროს რიცხვი ფრიად დიდ როლს ასრულებს მთელ მოლეკულურ ფიზიკაში და უნივერსალურ მუდმივას წარმოადგენს. -ისა არსებობს ავოგადროს რიცხვის განსაზღვრის ბევრი ისეთი მეთოდი რომლებიც არ საჭიროებს ატომის მასის პოვნას. ყველა ეს მეთოდი ერთსა და იმავე შედეგს გვაძლევს. ავოგადროს რიცხვი ფრიად დიდ როლს ასრულებს მთელ მოლეკულურ ფიზიკაში და უნივერსალურ მუდმივას წარმოადგენს.
მოლური მასა. ფარდობით მოლეკულურ მასასთან (Mფ) ერთად ფიზიკასა და ქიმიაში ფართოდ იყენებენ მოლურ მასას (M). მოლური მასა ეწოდებ 1 მოლი ნივთიერების მასას. ამ განსაზღვრის მიხედვით მოლური მასა ტოლია მოლეკულის მასის ნამრავლსა ავოგადროს რიცხვზე:

მოლური მასა (M)შეიძლება გამოვსახოთ ფარდობითი მასითაც. (1.5)_ში ჩავსვათ m0(1.2)_დან და NA (1.4)_დან, მივიღებთ.

მაგალითად, ნახშირმჟავა აირის ( ) მოლური მასაა 0,044 კგ/მოლი რადგან ნახშირმჟავა აირის ფარდობითი მოლეკულური მასა მიახლოებით ტოლი 44 – ის.თუ გავითვალისწინებთ (1.3) ფორმულას, ნებისმიერი ν ნივთიერების რაოდენობის m მასისათვის მივიღებთ ტოლობას: ) მოლური მასაა 0,044 კგ/მოლი რადგან ნახშირმჟავა აირის ფარდობითი მოლეკულური მასა მიახლოებით ტოლი 44 – ის.თუ გავითვალისწინებთ (1.3) ფორმულას, ნებისმიერი ν ნივთიერების რაოდენობის m მასისათვის მივიღებთ ტოლობას:

მაგალითად 3 მოლი ნახშირმჟავა აირის მასა ტოლია: m=3 მოლი·0,044 კგ/მოლი=0,132კგ.
მოლეკულური ფიზიკის ამოცანათა უმეტესი ნაწილის ამოხსნისათვის საჭიროა ვიცოდეთ ნივთიერების მოლური M მასის განსაზღვრა. ამისათვის მენდელეევის ცხრილიდან ცნობილი ფარდობითი ატომური მასების მიხედვით უნდა განვსაზღვროთ ფარდობითი Mფ მოლეკულური მასა, შემდეგ კი მოლური მასა, M=10¯3·Mფ კგ/მოლი ფორმულით, სადაც M მოლური მასაა, Mფ ფარდობითი მოლეკულური მასა.ხშირად საჭიროა სხეულის მოცემული მასის მიხედვით განისაზღვროს ნივთიერების რაოდენობა ან მოლეკულათა (ატომთა) რიცხვი. ამისათვის გამოიყენება ფორმულები:
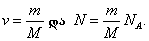
ცალკეულ მოლეკულათა მასა განისაზღვრება M0=M/NA ფორმულით. ზოგიერთ ამოცანაში ნივთიერების მასა უნდა გამოვსახოთ მისი ρ სიმკვრივით და V მოცულობით m=ρV; მოვიყვანოთ მაგალითები:
ამოცანა №1
განვსაზღვროთ წყლის მოლური მასა.
ამოხსნა.
წყლის ქიმიური ფორმულაა H2O, წყალბადის ფარდობითი ატომური მასა არის 1,00797 ჟანგბადისა კი 15,9994. მაშასადამე, წყლის ფარდობითი მოლეკულური მასა
Mფ=2· 1,00797 +15,9994=18,01534=18. წყლის მოლური მასა M=Mფ ·10¯3 კგ/მოლი=18·10¯3 კგ/მოლი=0,018კგ/მოლი.
პასუხი: Mფ=0,018კგ/მოლი.
ამოცანა №2
გავსაზღვროთ ნივთიერების რაოდენობა და მოლეკულების რიცხვი 1 კგ(m=1კგ.) ნახშირორჟანგში.
ამოხსნა.
ნახშირორჟანგის ქიმიური ფორმულაა CO2, ნახშირბადის ფარდობითი ატომური მასა არის 12, ჟანგბადისა კი 2·15,9994 =32. ნახშირორჟანგის ფარდობითი მოლეკულური მასა იქნება Mფ=12+32=44. მაშასადამე ნახშირორჟანგის მოლური მასა M=Mფ ·10¯3 კგ/მოლი=44·10¯3 კგ/მოლი=0,044კგ/მოლი. რადგან ნახშირორჟანგის მოლური მასა M=0,044კგ/მოლი, ამიტომ ნივთიერების რაოდენობა
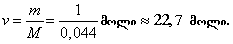
მოლეკულების რიცხვი.
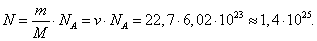
პასუხი: N = 1,4 ·10 25
| 






